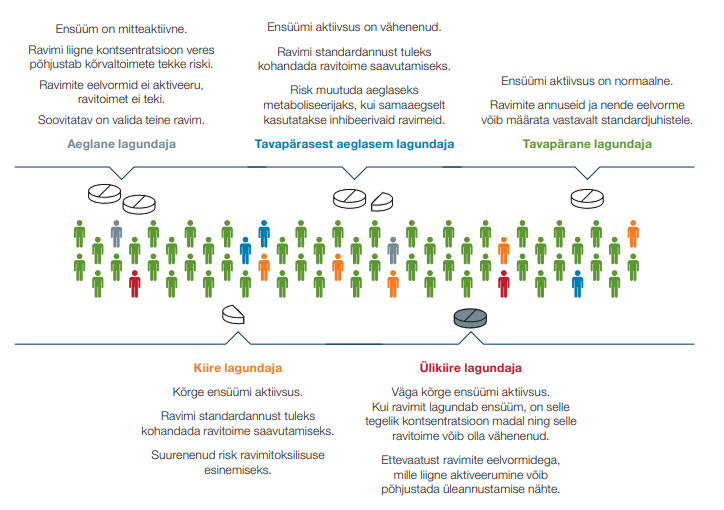
Üks ravim samas annuses ei sobi kõigile ühtmoodi – mõnele efektiivne ravimiannus võib teisele ravitoimet mitte avaldada, põhjustada tõsiseid kõrvaltoimeid või osutuda eluohtlikuks. Kuni 20% ambulatoorsetel patsientidel esineb ravimite suhtes kõrvaltoimeid ning 10-20% statsionaarsetel patsientidel esineb hospitaliseerimise ajal vähemalt üks kõrvaltoime.
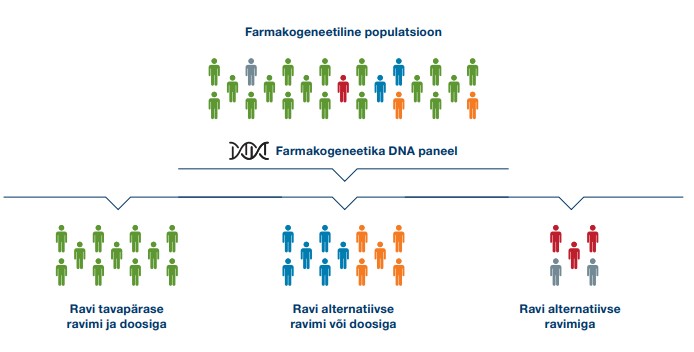
Farmakogeneetika DNA paneel võimaldab uurida patsiendi personaalset geeniprofiili ning vastavalt sellele määrata sobivad ravimid õiges annuses, suurendades seeläbi ravi õnnestumise tõenäosust ning vähendades ohtlike kõrvaltoimete või ebatõhusa ravi riski.
>> Vaata tulemuste raportis sisalduvaid toimeaineid
- Organismis ravimite toimet mõjutavate geenivariantide määratlemine ja geeni ning ravitoime vaheliste seoste selgitamine.
- Tõsiste ravimi kõrvaltoimete ning ravimite koostoimete ennetamine.
- Optimaalse raviplaani koostamine vastavalt patsiendi unikaalsele geneetilisele informatsioonile.
- Üldlevinud ravimivalikute ning katse- ja eksitusmeetodil põhinevate raviplaanide asendamine.
- Üldiste ravikulude vähendamine.
1.Teades patsiendi farmakogeneetilist profiili, võib arst suunatult ja kiiresti määrata patsiendile sobiva ravimi kohandatud annuses.
Patsiendi ravivastust tuleks arvestada kõikidel meditsiinierialadel. Farmakogeneetiliste analüüside kasutamine on eriti väärtuslik järgmiste ravimite puhul:
- antidepressandid ja muud psühhotroopsed ravimid;
- valuvaigistid/reumavastased ravimid;
- antikoagulandid;
- antibiootikumid, viiruse- ja seenevastased ravimid;
- diabeedivastased ravimid;
- hüpertensiooni vastased ravimid;
- tsütostaatikumid;
- prootonpumba inhibiitorid;
2. Ravi kvaliteet paraneb ja ravikulud vähenevad
3. Farmakogeneetiliselt testitud patsientidel täheldatakse:
- suuremat sümptomite leevenemise tõenäosust võrreldes tavapärase raviga;
- märkimisväärselt paremat ravivastuse määra ja talutavust;
- lühemat hospitaliseerimise aega;
- madalamaid ravikulusid.
4. Farmakogeneetiliselt testitud patsientidel, kes kasutavad samaaegselt mitut ravimit täheldatakse:
- vähenenud haiglaravi vajadust;
- vähenenud arstivisiite.
Mitmete geenide koosuurimine on kiirem ja kulutõhusam kui üksikute geenide eraldi uurimine. SYNLABi Farmakogeneetika DNA paneeli on kokku koondatud 34 geeni, mis on seotud ligi 300 ravimi toimeaine metabolismiga.
| Geen | Funktsioon |
| ABCB1 | Kodeerib P-glükoproteiini, mis on oluline rakumembraani transportvalk. P-glükoproteiin kontrollib ühendite sisenemist rakku üle terve organismi, mõjutades seeläbi ka ravimi kontsentratsiooni. |
| ABCG2 | Kodeerib raku membraani valku, mis viib mitmeid molekule, sh ravimid, üle membraani laiali. ABCG2 transpordib osaliselt samu ravimeid, mida P-glükoproteiingi. |
| BCHE | Kodeerib mittespetsiifilist butürüülkoliinesteraasi, mis hüdrolüüsib erinevaid koliinipõhiseid estreid. |
| CACNA1S | Kodeerib dihüdropüridiini retseptori alfa1S-alaühikut, mida ekspresseeritakse lihasrakkude sarkoplasmaatilises retiikulumis ning mis aktiveerib RYR1 kaltsiumikanali membraani depolarisatsiooni ajal kontraktiilsetes müotsüütides. |
| CYP1A2 | Hepaatiline ensüüm, mis vahendab mitmete ravimite, kofeiini ja prokartsinogeenide metabolismi. |
| CYP2B6 | Hepaatiline ensüüm, mis vastutav HIV-i ja vähiravimite ning bupropiooni metabolismi eest. |
| CYP2C rs12777823 |
Geneetiline variant, mida seostatakse väiksemate varfariini annustega. |
| CYP2C19 | Hepaatiline ensüüm, mis vahendab mitmete oluliste ravimite metabolismi, mille hulka kuuluvad psühhotroopsed ravimid ja maohappepumba blokaatorid ning antikoagulandid. |
| CYP2C8 | Hepaatiline ensüüm, mis vahendab mitmete ravimite metabolismi, mille hulka kuuluvad diabeedivastased ravimid, statiinid, valuvaigistid ja vähiravimid. |
| CYP2C9 | Hepaatiline ensüüm, mis vahendab mitmete ravimite metabolismi, mille hulka kuuluvad varfariin ja fenütoiin. |
| CYP2D6 | Hepaatiline ensüüm, mis vahendab ligikaudu 20-25% kasutusel olevate ravimite metabolismi, mille hulka kuuluvad antidepressandid, antipsühhootikumid, valuvaigistid. |
| CYP3A4 | Hepaatiline ensüüm, mis vahendab 30-50% kasutusel olevate ravimite metabolismi. |
| CYP3A5 | Hepaatiline ensüüm, mis vahendab mitmete ravimite metabolismi, millest olulisem on takroliimus. |
| CYP4F2 | Vahendab mitmesuguste endogeensete substraatide ja ksenobiootikumide metabolismi. Genotüübiteave võib olla kasulik nt varfariini annuse ennustamisel. |
| DPYD | Kodeerib dihüdropürimidiindehüdrogenaasi, mis kataboliseerib fluoropürimidiine, mida kasutatakse kemoterapeutikumidena erinevat tüüpi vähi korral. |
| F2 | Kodeerib protrombiini, mis on hüübimiskaskaadis üheks võtmeensüümiks. Protrombiini geeni mutatsioon soodustab tromboosi teket. |
| F5 | Kodeerib faktor V hüübimisfaktorit. F5 geeni mutatsioon (nn Leideni mutatsioon) on kõige sagedasem pärilikku tromboosi põhjustav mutatsioon. |
| G6PD | Kodeerib glükoos-6-fosfaatdehüdrogenaasi, mis kaitseb erütrotsüüte oksüdatiivse stressi eest. |
| HLA alleelid HLA-A*31:01, HLA-B*15:02, HLA-B*57:01 | HLA klass I alleelid kodeerivad MHC I molekule, mis esitavad peptiide CD8+ T-rakkudele. Teatud variandid, nagu HLA-A31:01, HLA-B15:02 ja HLA-B*57:01, suurendavad konkreetsete ravimite poolt indutseeritud T-rakuliste ülitundlikkusreaktsioonide riski, mis võivad väljenduda raskete naha- ja süsteemsete kõrvaltoimetena. |
| IFNL3 | Kodeerib interferooni lambda 3, mis vallandub viirusinfektsioonide kõrval. Selle geeni variandid aitavad hinnata C-hepatiidi ravi efektiivsust. |
| MT-RNR1 | Mitokondriaalne geen, mis kodeerib 12S rRNA-d ning mõjutab mitokondriaalse ribosoomi talitlust. Genotüübi andmeid kasutatakse aminoglükosiidide ohutuse hindamiseks ja ravi individualiseerimiseks, kuna teatud variandid suurendavad tundlikkust aminoglükosiidantibiootikumide suhtes. |
| MTHFR | Kodeerib metüleentetrahüdrofolaadi reduktaasi ensüümi, mis omab kriitilist rolli folaadi metabolismis ning mõjutab metüülimist ja DNA sünteesi radasid. |
| NAT2 | Atsetüleerib ja neutraliseerib mitmeid võõrühendeid. Osaliselt aktiveerib ja tekitab teatud kantserogeene, mille aktiivsus võib olla seotud vähiriskiga (nt eesnäärme- või kolorektaalvähk). |
| NFIB | Kodeerib mitmes koes ekspresseeritavat transkriptsioonifaktorit. Geen asub 9. kromosoomi lühikeses õlas. Selles piirkonnas asuvad koopiaarvu variandid põhjustavad MACID-sündroomi tekkimist (makrotsefaalia ja intellektuaalse arengu häired) ning selle geenisiseseid variante on seostatud klosapiini metabolismiga. |
| NUDT15 | Kodeerib nukleosiiddifosfataasi ensüümi, mis muudab tiopuriini ravimite metaboliidid vähem tsütotoksiliseks vormiks. |
| RARG | Kodeerib retinoehappe retseptorit γ, mis reguleerib geeniekspressiooni ja rakutalitlust. Farmakogeneetiliselt on RARG seotud all-trans retinoehappe (ATRA) ravivastusega teatud leukeemiatüüpides, mõjutades ravi efektiivsust ja kõrvaltoimete riski. Variandid selles geenis võivad mõjutada ravivastust. |
| SLCO1B1 | Kodeerib OATP1B1 valku, mis hõlbustab plasmast statiinide omastamist maksas. |
| SLC28A3 | Kodeerib nukleosiidide transporterit, mis mõjutab ravimite rakkudesse sisenemist. Geenivariandid võivad muuta nukleosiidide analoogide (nt teatud vähiravi ja HIV-ravimid) ja mõnede südameravimite taluvust ja kõrvaltoimete riski. |
| TPMT | Kodeerib tiopuriinmetüültransferaasi, mis vastutab tiopuriini ravimite metabolismi eest. |
| UGT1A1 | Kodeerib ensüümi UDP-glükuronosüültransferaas 1-1, mis vastutab teatud ravimite (nt vähivastased ravimid) metaboliseerimise ja bilirubiini eliminatsiooni eest. |
| UGT1A6 | Kodeerib ensüümi UDP-glükuronüültransferaasi 1A6, mis osaleb ravimite ja endogeensete ühendite glükuronimisprotsessis, muutes need kergemini erituvaks. Farmakogeneetiliselt võivad UGT1A6 variandid mõjutada teatud ravimite metabolismi kiirust ja toksilisust. |
| VKORC1 | Osaleb hüübimisfaktorite aktiveerimises ning omab pärilikke vorme, mis mõjutavad otseselt varfariini doseerimist. |
Farmakogeneetiline analüüs ei nõua tänapäeval spetsiifilist preanalüütikat ega erilist proovivõttu. Patsient loovutab tavapärase veenivere andmise protseduuri käigus ühe katsuti verd. Proov transporditakse laborisse, kust saab alguse analüüsi tegemine.
Analüüsi tulemusel valmib üksikasjalik raport, mis sisaldab lisaks geenispetsiifilistele tulemustele veel põhjalikku ravimite ülevaadet koos annustamissoovitustega ning kokkuvõtet testitud geenidest ja prognoositud fenotüüpidest. Raportit on võimalik vaadata eesti, inglise, soome, prantsuse, saksa, rootsi ja hollandi keeles.
Proovivõtt → DNA eraldamine → OpenArray ja CNV analüüs → Interpretatsioon
Genotüüpide toorandmed organiseeritakse geenide järgi. Informatsiooni täpsuse ja kaasaegsuse eest vastutavad mitmed meditsiinispetsialistid. Raport sisaldab:
Paneelis sisalduvad geenid on seotud ligi 300 ravimi toimeaine metabolismiga, mis on seotud erinevate terapeutiliste valdkondadega.
Ravimid grupeeritakse tulemuste alusel:
- olulise kliinilise tähtsusega geneetilise variatsiooniga ravimid;
- teatud kliinilise tähtsusega geneetilise variatsiooniga ravimid;
- vähese kliinilise tähtsusega geneetilise variatsiooniga ravimid;
- ravimid, millel puuduvad kliiniliselt olulised geneetilised variatsioonid.
Raportis on eraldi välja toodud ka tugevalt mõjutatud ravimid erineva terapeutilise valdkonna kohta koos toimeaine ja fenotüübiga.
Valdkonnad, kuhu farmakogeneetika uuringus sisalduvad toimeained kuuluvad:
- Dermatoloogias kasutatavad ained
- Hingamissüsteem
- Infektsioonivastased ained süsteemseks kasutamiseks
- Kardiovaskulaarsüsteem
- Kasvajavastased ja immunomoduleerivad ained
- Meeleelundid
- Närvisüsteem
- Parasiidivastased ained, insektitsiidid ja Repellendid
- Seedekulgla ja ainevahetus
- Skeleti-lihassüsteem
- Süsteemsed hormoonpreparaadid, va suguhormoonid ja insuliinid
- Urogenitaalsüsteem ja suguhormoonid
- Veri ja vereloomeorganid
- Muu
Vaata raportis sisalduvaid toimeaineid koos terapeutiliste valdkondadega SIIN (PDF).
Seda, kas huvipakkuv ravim või toimeaine sisaldub raportis, saad mugavalt kontrollida SIIN lingil.
Iga ravimi juures on teaduslikel andmebaasidel (CPIC jt) põhinevad ravimispetsiifilised annustamissoovitused. Soovitused on klassifitseeritud ravimi ohutuse alusel:
![]() Farmakogeneetiline mitmekesisus mõjutab ravimite tõhusust või kõrvaltoimeid kliiniliselt olulisel määral. Soovitatav on teha geenianalüüs. Enne ravimi määramist kontrollige olemasolevaid analüüsitulemusi. Kontrollige analüüsitulemuste põhjal annuseid ja manustamist.
Farmakogeneetiline mitmekesisus mõjutab ravimite tõhusust või kõrvaltoimeid kliiniliselt olulisel määral. Soovitatav on teha geenianalüüs. Enne ravimi määramist kontrollige olemasolevaid analüüsitulemusi. Kontrollige analüüsitulemuste põhjal annuseid ja manustamist.
![]() Farmakogeneetiline mitmekesisus mõjutab ravimite tõhusust või kõrvaltoimeid, mis on mõningal määral kliiniliselt oluline. Kui geenianalüüsi tulemused on olemas, kaaluge tulemuste põhjal ravimite või annuste kohandamist. Kui geenianalüüsi ei ole tehtud, kaaluge selle tellimist.
Farmakogeneetiline mitmekesisus mõjutab ravimite tõhusust või kõrvaltoimeid, mis on mõningal määral kliiniliselt oluline. Kui geenianalüüsi tulemused on olemas, kaaluge tulemuste põhjal ravimite või annuste kohandamist. Kui geenianalüüsi ei ole tehtud, kaaluge selle tellimist.
Farmakogeneetiline mitmekesisus võib mõjutada ravimite tõhusust või kõrvaltoimeid, kuid see on enamiku patsientide puhul kliiniliselt ebaoluline. Jälgige ravivastust ja võimalikke kõrvaltoimeid. Kui geenianalüüsi tulemused on olemas, kaaluge tulemuste põhjal ravimite või annuste kohandamist.
![]() Farmakogeneetiline mitmekesisus ei mõjuta märkimisväärselt ravimite tõhusust ega kõrvaltoimeid.
Farmakogeneetiline mitmekesisus ei mõjuta märkimisväärselt ravimite tõhusust ega kõrvaltoimeid.
Farmakogeneetika DNA paneel on näidustatud järgmistel juhtudel:
- ravimravi alustamine;
- sobiva annuse määramine;
- kahtlus ravimite efektiivsuses;
- ravimi kõrvaltoimete ennetamine.
Uuritav materjal: EDTA-veri, suu limaskesta kaabe
Materjali säilitamine: toatemperatuuril 24h; 2-8 °C 5 päeva; kauem sügavkülmutatult.
Vastuse saamise (TAT) aeg: 21 tööpäeva
Hind: 315 € (TK koodid 66616 ja 66610×2)
Farmakogeneetika DNA paneeli on võimalik tellida:
- Arstina patsiendile elektroonselt arsti programmist või pabersaatekirjaga
Elektroonset saatekirja saab vormistada arsti programmist, millel on eelnevalt SYNLABiga liidestus loodud läbi Medipost andmevahetusplatvormi. Hetkel on aktiivsed liidesed programmidega Perearst2, Perearst3, LIISA, eKliinik, Watson/Winston, Ester/Heda, MIS.
Analüüs on leitav SYNLABi nimekirjast uuringugrupist „Pärilike haiguste, riskialleelide uuringud“ nimega „Farmakogeneetika DNA paneel“:
- Valige topeltklikiga analüüs
- Sisestage õigesse lahtrisse ribakoodi number ning kuupäev ja kellaaeg
- Vajutage sõltuvalt programmist „Salvesta“ ja „Saada“ või „Esita“
Programmi sisestatud ribakood tuleb kleepida katsuti etiketile vertikaalselt. Kui Teie asutus ei kasuta ribakoode, palume sisestada arsti programmi kuupäeva ja kellaaja ning printida otse programmist välja saatekiri. Katsuti markeerida sellisel juhul patsiendi nimega nii nagu saatekirjal.
Programmi või elektroonse tellimise võimaluse puudumisel saab vormistada pabersaatekirja (arvutis täidetav versioon või trükitav versioon). Saatekirjal on vaja täita patsiendi ja tellija andmed, lisaks ka proovivõtu kuupäev ja kellaaeg. Analüüside nimekirjast märkida „Farmakogeneetika DNA paneel“.
Proovide logistika SYNLAB Tallinna molekulaarbioloogia laborisse korraldab SYNLAB. Kui proovivõttu Teie asutuses ei toimu, on võimalik patsient suunata SYNLABi verevõtupunktidesse. Verevõtuks aega broneerima ei pea, teenindatakse elava järjekorra alusel. Oluline on, et tellimus on eelnevalt arsti programmis tehtud või patsiendile saatekiri kaasa antud.
Kui analüüs on valmis, edastatakse arve suunavale kliinikule. Kui soovite, et patsient tasuks analüüsi eest laboris kohapeal, palume kasutada isemaksja saatekirja.
- Erakliendina Minu SYNLABist
- Pharmacogenetics: The right drug for you | Nature
- Meta-analysis of probability estimates of worldwide variation of CYP2D6 and CYP2C19 | Translational Psychiatry (nature.com)
- Pharmacogenetic testing among patients with mood and anxiety disorders is associated with decreased utilization and cost: A propensity‐score matched study – Perlis – 2018 – Depression and Anxiety – Wiley Online Library
- Incidence, preventability, and causality of adverse drug reactions at a university hospital emergency department | SpringerLink
- https://www.tai.ee/et/personaalmeditsiini-uudiskirjad/uuringud-farmakogeneetiline-testimine-aitab-ravi-tohusamaks-muuta
- Using pharmacogenetic testing in psychiatry, Jari Forsström, Chief Medical Officer, Abomics Oy
Vaata videomaterjali meie e-koolituskeskusest klikkides allolevale nupule: